PRP GROWTH FACTOR INJECTIONS
MAGNOVISION THERAPY
PHOTOBIOMODULATION THERAPY
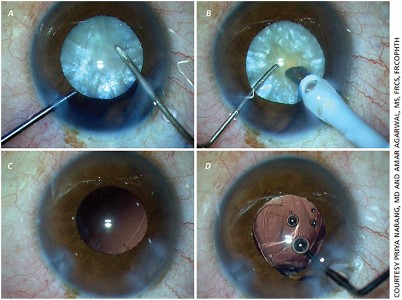
ARGUS II RETINAL PROSTHESIS OPERATION
Der Augapfel besteht aus refraktiven Einstellungen, die das Licht von vorne nach hinten auf die Netzhaut fokussieren. Die Hornhaut liegt vorne und die Linse dahinter bündelt das Licht auf der Netzhaut.
Der Augapfel besteht von innen nach außen aus 3 Schichten. Die innerste Netzhaut ist die Gefäßschicht in der Mitte, und die äußerste ist das Weiß des Auges, das dem Augapfel seine Steifigkeit verleiht.
Objekte können gesehen werden, wenn die von den Objekten ausgehenden Strahlen auf der Netzhaut fokussieren. In der Netzhaut befinden sich Zellen, die Lichtenergie in elektrische Energie umwandeln und an das Gehirn weiterleiten. Diese werden Photorezeptoren genannt. Photorezeptoren bestehen aus zwei Gruppen:
Kegelzellen: Bilder, die in der Mitte und in einer hellen Umgebung entstehen,
Stäbchenzellen: verarbeitet Bilder, die in der Umgebung und in der dunklen Umgebung entstehen.
Mit anderen Worten, sie wandeln die von den Objekten kommenden Strahlen in elektrische Energie um.
Elektronenmikroskopische Ansicht des Netzhautschnitts. Knapp über dem untersten Pigmentepithel befinden sich Photorezeptorzellen, die aus Stäbchen und Zapfen bestehen.
Retinitis pigmentosa beginnt mit einer Mutation oder einem Defekt in den Genen von Photorezeptorzellen.
250 verschiedene genetische Mutationen führen zu 50 verschiedenen Arten dieser Krankheit. Aus diesem Grund sind die klinischen Symptome und die Progressionsrate bei jedem Patienten unterschiedlich. Es ist in der Regel familiär aufgrund von Blutsverwandtschaft, kann aber auch nicht familiär auftreten.
Genetische Mutation führt zu vorzeitiger Alterung und fortschreitendem Tod von Photorezeptorzellen. Mit zunehmendem Alter beschleunigt sich der Zelltod.
Wachstumsfaktoren ermöglichen die Umwandlung von Glukose im Blut in ATP-GTP, den Zellbrennstoff. In Abwesenheit von Wachstumsfaktoren verlangsamen Photorezeptorzellen aufgrund von Energiemangel ihre Stoffwechselaktivitäten, gehen in den Schlafmodus, und wenn der Prozess fortgesetzt wird, tritt der Zelltod fortschreitend ein.
Die Wachstumsfaktoren, die die Photorezeptoren am Leben erhalten, werden nicht vom Pigmentepithel und den Müllerzellen ausgeschieden, die Stammzelleigenschaften aufweisen. Fotorezeptoren gehen für lange Zeit in den Schlafmodus, bevor sie langsam absterben. In diesem Stadium leben die Zellen, sind aber nicht an der Sehfunktion beteiligt.
Welche Zellen zuerst in den Schlafmodus gehen oder sterben, beginnen die Symptome entsprechend. Wenn zum Beispiel die Stäbchenzellen zuerst zu sterben beginnen, ist das erste Symptom eine verminderte Nachtsicht.
Bei einigen genetischen Typen der Krankheit sind Zapfenzellen betroffen, bevor Stäbchenzellen betroffen sind. Die Zapfenzellen gehen zunächst in den Schlafmodus und sterben dann ab.
Dieser Zustand wird bei der Stargarth-Krankheit, der reversen rp oder der Zapfendystrophie beobachtet.
Hier ist das erste Symptom eine übermäßige Blendung im Licht und eine bessere Sicht in dunklen Umgebungen und bei Nacht. Mit fortschreitender Krankheit geht das zentrale Sehen verloren und das periphere Sehen bleibt erhalten.
Behandlung von Retinitis pigmentosa:
1) Stammzell- und Gentherapie:
Seine Studien sind noch im Gange und die Zielgruppe ist die Patientengruppe, die ihr Augenlicht nicht vollständig verloren hat und über lebende Zellen im Schlafmodus verfügt. Das Grundprinzip der Stammzelltherapie besteht darin, Zellen, die in der Lage sind, Wachstumsfaktoren zwischen 6 Monaten und 2 Jahren abzusondern, in oder um das Auge herum zu injizieren und diesen Vorgang alle 6 Monate oder 2 Jahre zu wiederholen.
Bei der Gentherapie wird das fehlerhafte Gen in Photorezeptoren, die ihre Vitalität nicht verloren haben, erkannt, das korrigierte Gen in Viren geladen und ins Auge injiziert. Das Ziel ist wiederum, das Absterben lebender Photorezeptoren zu stoppen.
2) Früherkennung:
Je früher die Diagnose gestellt wird, kann das Absterben der verbliebenen Zellen ohne weiteren Verlust von Photorezeptoren so weit wie möglich verlangsamt, gestoppt oder sogar Zellen im Schlafmodus geweckt werden.
3) Injektionen von Wachstumsfaktoren
Ngf, bdnf, bfgf, IL6 sind Wachstumsfaktoren, die für Photorezeptoren notwendig sind, um ihre Vitalität und Funktion aufrechtzuerhalten.
Eine Erstbelastung und anschließende Wiederinjektion in bestimmten Abständen kann den Krankheitsverlauf verlangsamen oder stoppen. In einigen Fällen können je nach Vorhandensein oder Anzahl der Zellen im Schlafmodus die Gesichtsfelderweiterung und die Sehschärfe erhöht sein.
Vergrößerung des Gesichtsfeldes nach der 3. Injektion
4) Okuvision und Magnovision
Die elektromagnetische Stimulation der Netzhaut und des Sehzentrums im Gehirn erhöht nicht nur die Sekretion der notwendigen Wachstumsfaktoren im Nervensystem, sondern ermöglicht auch die Bildung neuer Sehbahnen, die als neuronale Plastizität bezeichnet werden, und die Reorganisation der Sehfunktion.
Das Erwachen der Photorezeptoren im Schlafmodus und die Vergrößerung des Gesichtsfelds bei dem Patienten, der sich einer Wachstumsfaktorinjektion zusammen mit Magnovision unterzogen hatte, sind in der folgenden Abbildung dargestellt.
5) Behandlung von Komplikationen
Katarakt entwickelt sich häufig bei rp-Patienten. In fortgeschrittenen Stadien werden die Netzhautgefäße dünner und Sauerstoff erreicht das intraokulare Gewebe und essentielle Nährstoffe nehmen ab. Dies beschleunigt die Entwicklung von grauem Star.
Kataraktoperationen bei rp-Patienten können den Zelltod in der Netzhaut beschleunigen und eine übermäßige Zunahme des Makulaödems verursachen. Aus diesem Grund minimiert der Schutz der Netzhaut mit Wachstumsfaktoren vor der Kataraktoperation die möglichen Risiken.
Makulaödem ist eine weitere häufige Komplikation bei rp-Patienten. Ein Ödem auf einem bestimmten Niveau erfordert keine Behandlung, da es die Wachstumsfaktoranforderungen für Photorezeptoren erfüllt. Ödeme, die die Sehschärfe beeinträchtigen und zystoide werden, erfordern jedoch eine Behandlung. Wenn es nicht mit Augentropfen kontrolliert werden kann, sollte das Ödem mit intraokularen Injektionen kontrolliert werden.
6) Schutzbrille
Das Filtern von blau-violettem Licht bei einer Wellenlänge von 415-455 nm reduziert die Todesrate der Photorezeptoren um 25 %. Es wird besonders für Computerbenutzer empfohlen.
Orangefarbene 500-nm-Linsen werden für rp-Patienten mit anfänglicher Katarakt oder übermäßiger Blendung im Licht empfohlen, wo auch Zapfenzellen betroffen sind.
7) Rehabilitationsinstrumente für Sehbehinderte:
Bei Patienten, deren Zapfenzellen betroffen sind und bei denen das periphere Sehen gut ist, sprechen Fernrohrbrillen, Lupen mit Licht oder Lupen mit Überwachungskameras besonders gut auf das Lesebedürfnis der Patienten an.
8) Implantation einer intraokularen Teleskoplinse:
Prismatische teleskopische Intraokularlinsen, die das Bild aus dem toten Bereich verlagern, liefern bei geeigneten Patienten zufriedenstellende Ergebnisse bei Patienten mit Zapfenzellbefall und gutem peripherem Sehen.
9) Ernährung-gesundes Leben:
Es ist möglich, die Todesrate von Photorezeptoren zu verlangsamen, indem man Lebensmittel mit einem hohen Gehalt an antioxidativen Vitaminen und Mineralien sowie Nahrungsergänzungsmitteln zu sich nimmt. B12-b6-b1-Folsäure und Omega-3 sind besonders notwendig für die lebenswichtigen Aktivitäten von Nervenzellen, während Vitamin a-Lutein-Carotin für die Synthese von Pigmenten notwendig ist, die für die visuelle Funktion von Photorezeptoren notwendig sind.
Mediterrane Ernährung
Gegrillter Lachs: 2 Tage die Woche (alle fetten Fische – vorausgesetzt, sie werden gegrillt oder gebacken) (gebratener Fisch hat keine Vorteile.)
Viel grüner Salat + geriebene Karotten
Weich gekochte Eier: 3 Tage die Woche (gekochte Eier in Aprikosenkonsistenz)
Rosinen mit schwarzen Kernen oder frische schwarze Weintrauben je nach Saison: einmal pro Woche eine Handvoll
Rohe Mandeln: einmal wöchentlich eine Handvoll
Walnuss: einmal pro Woche, eine Handvoll
Kefir: 2 Tage die Woche, 1 Glas
Täglich 30 Minuten im Freien spazieren gehen
Absolut nicht rauchen
Abstinenz von Alkohol
Es wird die Todesrate von Photorezeptoren stark verlangsamen.
10) Für Patienten, deren Photorezeptoren ihre Vitalität vollständig verloren haben:
Virtuelles Sehen und Rehabilitation mit Chips zur Erfüllung der Funktion von Fotorezeptoren.
Das Bild wird von einer Kamera aufgenommen – in elektrische Energie umgewandelt und über Elektroden an das Gehirn weitergeleitet. Dafür,
Brainport v200
Argus 2 bionische Augen
kortikale Prothese
Die am besten geeignete Methode wird auf den entsprechenden Patienten angewendet.